双原子|《张朝阳的物理课》气体比热随温而变?探究双原子分子比热问题
2月13日12时,《张朝阳的物理课》第二十八期准时开播。搜狐创始人、董事局主席兼CEO张朝阳坐镇搜狐视频直播间,探究双原子分子的比热问题。他向网友介绍比热的概念,先推导单原子理想气体的比热,再利用能量均分定理推导双原子分子的比热,但与实验在室温下测得的数据不符。为了解释实验上观察到的定容比热随温度的阶梯变化,张朝阳引入了量子力学中分立能量的概念,以氢气与一氧化碳为例解释了阶梯曲线。最后利用玻尔兹曼分布与谐振子能级,计算了包含零点能的振动能平均能量,导出振动能对应的比热,与比热阶梯图在温度较高时的曲线变化一致。

文章插图
“我们的课程有很丰富的内容,如果不复习的话,还是有一定的难度。”今天开讲之前,张朝阳提醒网友学习物理要勤加复习,“一定要下载搜狐视频App。”他继续说,“我们还是学点物理吧,尽管有点费脑,但它是真实的、重大的,跟我们每个人的生活息息相关。”
经典力学的比热:比热依赖自由度 能量均分是基础
本节课张朝阳带着网友先研究摩尔比热容问题。摩尔比热容是1mol物质温度升高1K所需的热量,分为定容比热容和定压比热容。在温度升高的前提下,前者要求物体体积不变,后者要求压强不变。一般升高温度时,为了保持压强不变需要膨胀体积,物体对外做功会消耗内能,所以升高同样温度时,定压情况会比定容情况吸收更多的热量,即定压比热容一般会比定容比热容大。张朝阳介绍,这里只考虑定容摩尔比热容,为了方便,统称为定容比热。
“先来看单原子理想气体的比热情况。” 他提示,在温度为T时,根据能量均分定理,每个原子在每个自由度上具有1/2kT的能量,其中k是玻尔兹曼常数。那么一个方向上的动能具有1/2kT的能量,由于这里的理想气体是三维的,有三个方向,一共有3/2kT的能量,那么N个原子组成的气体的总内能是:
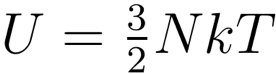
文章插图
将粒子数N用摩尔数n与阿伏伽德罗常数A表示为N=nA,则内能用摩尔数表示为:
其中,R=kA为普适气体常数。那么计算1mol物质温度升高1K所需的热量就得到单原子理想气体的定容比热:
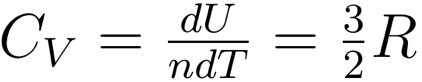
文章插图
讨论完单原子理想气体的比热后,张朝阳带领网友继续研究双原子分子理想气体的比热问题。同样根据能量均分定理,双原子分子每个自由度上分配1/2kT的能量,双原子分子有3个质心平动自由度,有2个转动自由度和1个振动自由度,除了动能自由度外,其振动对应的势能也可以储存能量,从而也贡献1个自由度,这样一共有7个自由度,那么单个分子的能量是7/2kT,类似单原子分子的计算,也可以求得双原子分子理想气体的定容比热是:
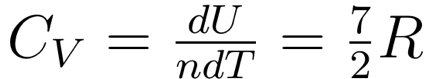
文章插图
遗憾的是,实验上测得的室温下双原子分子气体的定容比热并不是7/2R,而是5/2R。为什么会这样?他将悬念留在后面。
被“冻结”的自由度:转动振动逐级解冻 定容比热阶梯上升
张朝阳继续进行推导,“双原子分子气体的定容比热是随温度变化的,变化曲线像阶梯一样。”

文章插图
(定容比热随温度的阶梯图)
“要解释定容比热随温度的阶梯变化,就需要用到量子力学中能量分立的事实,以及玻尔兹曼分布的概念。”张朝阳介绍。玻尔兹曼分布是指粒子在不同能级上分布的概率满足:
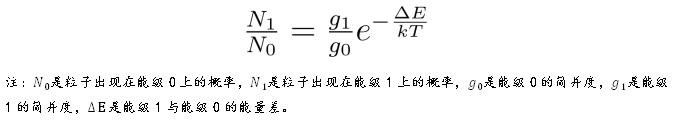
文章插图
若能级0为基态,由于能级能量在e指数上而且为负,粒子出现在某激发能级上的概率,随该能级能量的升高而快速下降。为了分析在室温下粒子处在激发态上的概率大小,张朝阳将kT用波数表示出来大约为200/cm,如果要激发的自由度的能量?E对应的波数比这个大得多,那么出现在这个自由度对应的激发能级上的概率将会非常小,分配到这部分自由度的能量将明显减少,不再像能量均分定理所说的那样平均分配。
【 双原子|《张朝阳的物理课》气体比热随温而变?探究双原子分子比热问题】张朝阳以一氧化碳为例,根据双原子分子转动能级角动量公式,激发其转动能对应的特征波数B大约为2/cm,比室温下的kT对应的波数要小得多,于是其转动能可以被比较完整地激发,满足能量均分定理。但激发一氧化碳振动能所对应的波数则远远大于室温下kT对应的波数,按照玻尔兹曼分布公式,粒子处在振动能激发态的概率会非常小,几乎都处于基态,其振动自由度被冻结,所以计算比热时可以忽略振动部分的2个自由度,从而室温下的比热的实验测定值就是5/2R。
- 机箱|内外设置精致双屏幕,二手金立w900体验,国产翻盖手机中的贵族
- ipad air|南孚电池遇“危机”?小米、飞利浦双双登场,成本不足1元有效期10年
- iqoo neo|iQOO“双机”降价,均搭载骁龙888处理器,到底该怎么选?
- |全新OriginOS Ocean操作方式优化升级,原子组件让出行更省心
- 荣耀|荣耀悄悄上架新机,120Hz双曲面屏+66W快充,起售价2199元
- 半导体|韩国三星去年半导体销售额和设备投资额,双双居全球首位,设备投资额2320亿元
- iqoo|120W快充,iqoo9还是降价了,六个平台双冠为什么降价这么快
- iqoo|iQOO 9开始降价,斩获六个“双冠王”
- 华为mate|鸿蒙3.0+100W快充+环形双主摄,华为Mate新机亮相,值得期待!
- 荣耀|双曲面流光幻镜,荣耀60 SE堪称2000元档手机颜值屏幕天花板
